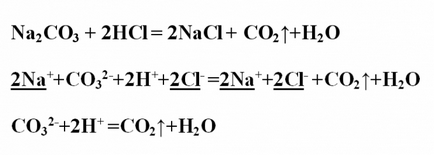Hogyan írjunk ionos egyenletek
Megkezdése előtt írásban ionos egyenletek, meg kell tanulni néhány szabályt. Vízben és malodissotsiiruyuschie gáznemű anyag (például víz) ionokra nem bomlanak, és ezért, felveszi a molekuláris formában. Itt is vannak gyenge elektrolitok, mint a H2S, H2CO3, H2SO3, NH4OH. A vegyületek oldékonyságát megtalálható a oldhatósága a táblázat, amely egy engedélyezett referencia anyag mindenféle kontroll. Ott kapnak az összes díjat, melyek velejárói kationok és anionok. A teljes körű végrehajtása a munkát, ha írsz a molekuláris, ion és teljes ion rövidített egyenlet.
Példa № 1. írása közötti semlegesítési reakció kénsav és kálium-hidroxid, úgy vélik, hogy szempontjából TED (elektrolitos disszociáció elméletének). Kérjük, vegye figyelembe a reakció egyenletet molekuláris formában és intézkedik koeffitsienty.H2SO4 + 2KOH = K2SO4 + 2H2OProanaliziruyte kapott anyag oldhatóságukat és disszociációs. Minden a vegyületek vízben oldódnak, és ezért disszociál ionokra. Az egyetlen kivétel a víz, amely nem esik szét ionokra, ezért maradnak a molekuláris ion vide.Napishite teljes egyenletet, meg ugyanazokat az ionokat a bal és a jobb oldalon, és hangsúlyozzák. Csökkentése érdekében ugyanazokat az ionokat, kereszt ih.2H + + SO4 2- + 2K + + 2OH- = 2k + + SO4 2- + 2H2OV eredmény ionos rövidített egyenletet: 2H + + 2OH- = 2H2OKoeffitsienty formájában párokat is csökkenthető: H + + OH- = H2O
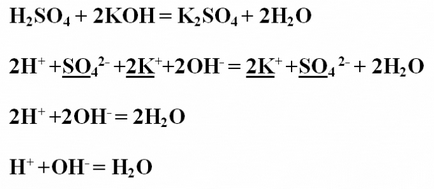
Példa № 2. Write cseréjét közötti reakció réz-klorid és nátrium-hidroxid, úgy vélik, hogy szempontjából a TED. Feljegyezzük a reakció egyenletet molekuláris formában és intézkedik a együtthatókat. Ennek eredményeként, a kapott réz-hidroxid kicsapódott kék. CuCl2 + 2NaOH = Cu (OH) 2 ↓ + 2NaClProanaliziruyte összes anyagot vízben való oldhatóságukat - oldható mindent, kivéve a réz-hidroxid, amely disszociál ionokra nem. Record ionos teljes egyenletet, a stressz és csökkenti az azonos ionok: Cu2 + + 2Cl- + 2Na + + 2OH- = Cu (OH) 2 ↓ + 2Na + + 2CI-ionos marad rövidített egyenletet: Cu2 + + 2OH- = Cu (OH) 2 ↓
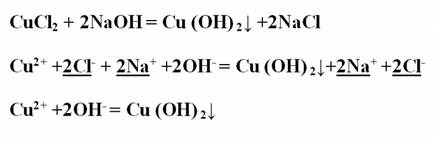
Példa № 3. Írja a csere közötti reakciót nátrium-karbonát és a sósav, úgy vélik, hogy szempontjából a TED. Feljegyezzük a reakció egyenletet molekuláris formában és intézkedik a együtthatókat. A reakció eredményeként nátrium-klorid és a felszabadult gáz alakú CO 2 (szén-dioxid vagy szén-monoxid (IV)). Ez alkotja bomlása a gyenge szénsav lebontó az oxid, és a víz. Na2CO3 + 2HCl = 2NaCl + CO2 ↑ + H2OProanaliziruyte összes anyagot a vízoldhatósága és a disszociációs. A szén-dioxid távozik a rendszerből, mint gáz halmazállapotú vegyület, víz - van malodissotsiiruyuschee anyag. Minden egyéb anyagok lebomlanak ionokra. Record ionos teljes egyenletet, a stressz és csökkenti az azonos ionok: 2Na + + SO3 2- + 2H + + 2Cl- = 2Na + + 2Cl- + CO2 ↑ + H2OOstaetsya ionos rövidítve egyenlet: SO3 2- + 2H + = CO2 ↑ + H2O